B、浓硝酸,稀硝酸具有强氧化性,遇金属反响不生成氢气而是构成氮的氧化物;
B、浓硝酸在常温下见光或受热会分化生成二氧化氮、水和氧气,与稀硝酸反响生成一氧化氮,故B过错;
C、铝在常温下遇浓硝酸产生钝化现象,阻挠反响进行,常温下可用铝制品盛装浓硝酸,而不是不反响,故C过错;
点评本题考察了硝酸性质的剖析使用,熟练掌握根底是解题要害,留意常温下铝、铁遇浓硝酸产生钝化,标题难度中等.
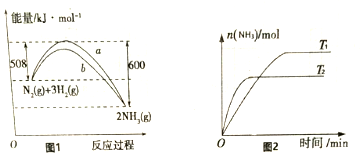
(g)△H=-92kJmol-1.(2)图1中改动某条件后,由曲线a变成曲线b,则改动的条件是.(3)依据图2判别T1和T2温度下的平衡常数巨细联系是K
分子中的H被-NH2替代的产品.发射卫星的火箭以N2H4(g)为燃料、NO2为氧化剂,二者反响生成N2和H2O(g).已知:N2(g)+2O2(g)=2NO2
彻底反响时放出的热量为113.57KJ.检查答案和解析科目:
题型:解答题16.如图为KNO3和NaCl的溶解度曲线,请答复下列问题:
(3)若固体KNO3中混有的少数NaCl,可采用降温结晶(填“蒸腾结晶”或“降温结晶“)的办法提纯.
(4)40℃时,将35.0gNaCl溶于100g水中,降温至0℃时,可分出晶体0g.